УДК 616.151.5
DOI: 10.32471 / umj.1680-3051.141.198615
За последние 70 лет произошли колоссальные изменения в подходах, оценке, доступности терапии и качества жизни пациентов с гемофилией. Если раньше основной целью лечения больных гемофилией было снижение риска смерти от неконтролируемой кровотечения, то сегодня все силы направлены на то, чтобы улучшить качество жизни больных. Однако, несмотря на все успехи в гематологии, до сих пор остается проблемным вопрос развития ингибиторной формы гемофилии (ИФГ) на фоне заместительной гемостатической терапии концентратами факторов свертывания крови VIII (IX). Согласно современным рекомендациям, лечение пациентов с ИФГ необходимо рассматривать в двух аспектах. Во-первых, в обеспечении гемостаза при острых геморрагических эпизодов и, во-вторых, полном удалении ингибитора [1]. Основным методом эрадикации ингибитора является, как известно, индукция иммунной толерантности (ИИТ), характеризующийся введением препаратов FVIII или FIX в высоких дозах до тех пор, пока организм не приучится распознавать лечения без реакции на него [2]. При успешном завершении этого курса лечения пациенты возвращаются на заместительную гемостатической терапии FVIII / FIX. Имеющиеся данные свидетельствуют, что ИИТ успешная в около 70% пациентов с ИФГ, обычно с низким / низькореагуючим ингибитором (0,6- <5 БУ / мл). В случае неэффективности ИИТ, например у пациентов с высоким / високореагуючим титром ингибитора (≥5 БУ / мл) или невозможности проведения ИИТ, пациентам с ИФГ лечения кровотечений можно проводить препаратами с «обходным» или шунтовым механизмом действия. К таким средствам относят два препарата: антиингибиторний коагуляционный комплекс (aPCC) и рекомбинантный активированный FVII (rFVIIа), которые имеют длительную историю применения, в частности как сопровождение ИИТ (табл. 1).
Таблица 1. Сравнение препаратов с шунтовым механизмом действия [6]
| Препараты из шунтовым механизмом действия | ||
|---|---|---|
| показатель | aPCC | rFVIIа |
| показания |
Лечение в случае спонтанных кровотечений у пациентов с ИФГ А и профилактики кровотечений при хирургических вмешательств. Профилактика кровотечений у больных с гемофилией А и высоким титром ингибитора и частыми гемартрозами |
Лечение в случае кровотечений у пациентов с ИФГ. Лечение в случае кровотечений из приобретенной гемофилией. Лечение в случае кровотечений у пациентов с Тромбастения Гланцмана |
| гемостатические компоненты | FII, FIX, FX, FVIIa, FXa | FVIIa |
| механизм действия | Активация FX и FII | Активация FX на поверхности тромбоцитов |
| Период полураспада, ч | 8-13 | 2-3 |
| Объем раствора для одной инфузии, мл | 90 | 5 |
| дозировка | 50-100 Ед. / Кг каждые 8-12 ч | 90-120 мкг / кг через 2-3 ч |
| Рекомендуемая доза для профилактики | 80 Ед. / Кг 3 раза в неделю | 90-270 мкг / кг / сут |
| Эффективность,% | 62 | 45-59 |
Лечение препаратами с шунтовым механизмом действия начинает свой отсчет с 1977, когда впервые на фармацевтический рынок Европейского Союза вышел препарат aPCC, в том же году он был включен в Боннской протокола ИИТ, в 1986 — утвержден к применению в США, а в 2013 получил разрешение FDA на профилактическое лечение гемофилии A и B у пациентов с ингибитором [3, 4]. Применение рекомбинантных препаратов начинает свой отсчет с начала 2000-х годов, когда на международном фармацевтическом рынке были представлены первые рекомбинантные препараты факторов свертывания крови, одним из которых был rFVIIа. Сегодня оба препарата зарекомендовали себя как эффективные средства в лечении эпизодов кровотечения у больных ИФГ [5].
Клинический эффект препаратов из шунтовым механизмом действия основан на индукции или восстановлении недостаточного тромбиноутворення, путем сложных взаимодействий с эндогенными факторами свертывания крови и тромбоцитами. aPCC по строению составляет проферментни формы прокоагулянтов, такие как FII, FVII, FIX и FX, а также следовые количества их активированных форм и антикоагулянтного белка С в физиологически сбалансированном соотношении. Кроме того, в его составе имеются небольшое количество коагуляционных кофакторних белков FV, FVIII и белка S, а также ингибитор пути тканевого фактора [7]. В комплексе все эти составляющие позволяют эффективно активировать систему плазменной гемостаза и, соответственно, вызвать гемостатический эффект в месте поражения сосуда (рис. 1).
Рисунок. Механизм действия aPCC.
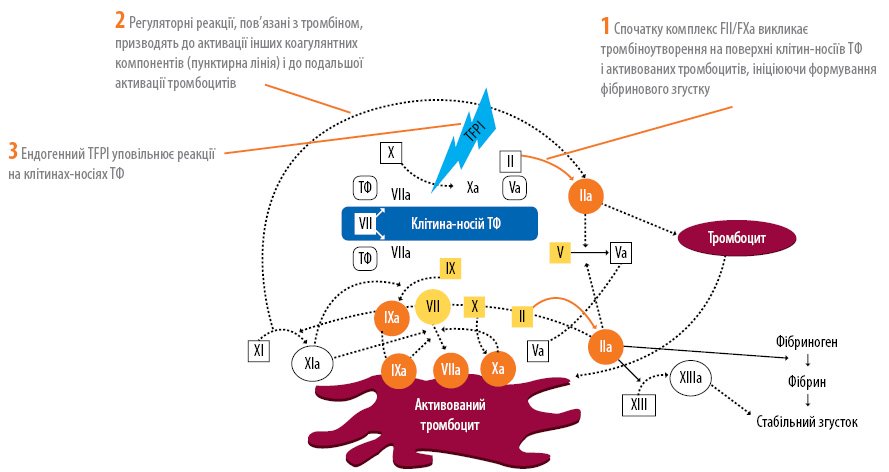
ТФ — тканевый фактор, TFPI — ингибитор пути тканевого фактора.
Механизмы, обеспечивающие гемостатическое воздействие aPCC:
- активация совместного пути свертывания в результате формирования и влияния протромбиназного комплекса;
- активация внутреннего пути свертывания, с помощью которого происходит тромбинзалежна активация по принципу обратной связи;
- активация внешнего пути гемостаза за счет FХa-зависимой активации FVII и последующей FVIIa-зависимой активации FX.
rFVIIа действует локально в месте повреждения сосуда, где выделяется тканевой фактор и оказываются активированы тромбоциты, инициирует процесс гемостаза, вызывая образование небольших количеств тромбина. Непосредственное действие rFVIIa представлена активацией FX на поверхности активированных тромбоцитов. FXa в комплексе с FVa вызывает образование большего количества тромбина, что в дальнейшем приводит к появлению стабильной гемостатической пробки в месте повреждения сосуда. Шунтовой механизм действия препарата реализуется за счет повышенной более чем в 1000 раз концентрации FVIIа в плазме крови.
Сегодня данные литературы свидетельствуют, что препараты с шунтовым механизмом действия являются эффективными средствами лечения в случае кровотечений у пациентов с ИФГ (табл. 2). Согласно результатам международных исследований, эффективность этих препаратов примерно одинакова и составляет около 80%, существенная разница заключается в периодах полураспада. Так, для препарата rFVIIa он составляет 2-3 ч, aPCC — 8-12 ч.
Таблица 2. Профилактическая терапия пациентов с ИФГ
| Рекомендуемые дозировки препаратов с шунтовым механизмом действия во время / вне ИИТ |
||
|---|---|---|
| показатель | Во время ИИТ | вне ИИТ |
| rFVIIа | Кратковременная профилактика до 3 мес в режиме дозирования 90 мкг / кг 1 раз в сутки | Кратковременная профилактика до 3 мес в режиме дозирования 90 мкг / кг 1 раз в сутки |
| aPCC | Доза 50-100 Ед. / Кг каждые 12 ч до снижения титра ингибитора <2 БУ | Доза 30-100 Ед. / Кг 3 раза в неделю или через день |
Очевидно, что эффективность препаратов связана с многофакторным механизмом их действия, обеспечивая тем самым высокую эффективность и продолжительность клинического эффекта препаратов, подтверждено рядом клинических исследований [8–11]. В частности, эффективность и безопасность aPCC по профилактике и устранению кровотечений у пациентов с ИФГ А и В подтверждено в проспективном мультицентровом исследовании Pro-FEIBA, результаты которого показали, что у пациентов, которым вводили aPCC в дозе 85 МЕ на 1 кг массы тела, отмечали существенное снижение частоты всех эпизодов кровотечений на 62%, гемартроза — на 61% и кровоизлияний в суставы-мишени — на 72% [12]. Результаты недавно проведенного исследования PROOF показали, что терапия aPCC в дозе 85 ± 15 МЕ ассоциированная со значительно меньшим количеством кровотечений — как при профилактическом, так и при эпизодическом введении препарата. Также результаты свидетельствуют, что aPCC значительно уменьшал количество спонтанных кровотечений, предотвращая тем самым развитию или прогрессированию гемофилической артропатии и улучшая качество жизни пациентов [13].
Гемартроз — одно из самых опасных осложнений гемофилии, что может привести к артропатии, которая является основной причиной заболеваемости и инвалидизации у пациентов с гемофилией. По сравнению с пациентами без ингибиторов пациенты с ИФГ не имеют повышенного риска кровотечений. Однако с их кровотечениями труднее справиться, что затрудняет лечение пациентов, особенно во время хирургического вмешательства и повышает риск развития осложнений, включая прогрессированием заболевания суставов до конечной стадии. Согласно современным рекомендациям, применение обходных (шунтирующих) препаратов является проверенным эффективным стандартом лечения пациентов с ингибиторами при операционных вмешательствах.
Таким образом, в случае неуспеваемости или невозможности проведения ИИТ у пациентов с ИФГ предотвращения кровотечений можно проводить препаратом из шунтовым механизмом действия, таким как aPCC, который имеет длительную историю применения и продолжает занимать важное место в комплексной терапии пациентов с ингибиторами и рекомендован для профилактического. Кроме того, современные рекомендации регламентируют назначение этих препаратов с шунтовым механизмом действия при хирургических вмешательствах, с целью снижения риска развития кровотечений у пациентов с ИФГ.
При поддержке ООО «Такеда Украина»
VV-MEDMAT-37955
Список литературы / References:
- 1. Krasivska VV, Stasyshyn OV (2012) Pathological inhibitors of blood coagulation: distribution, diagnosis, clinical manifestations and treatment. UMJ, 4: 162-168. (In Ukr.).
- 2. Brackmann H.-H., White 2nd GC, Berntorp E. et al. (2018) Immune tolerance induction: What have we learned over time? Haemophilia, 24 (Suppl. 3): 3-14. doi: 10.1111 / hae.13445
- 3. Rota M., Cortesi PA, Crea R. et al. (2017) Thromboembolic event rate in patients exposed to anti-inhibitor coagulant complex: a meta-analysis of 40-year published data. Blood Adv., 1 (26): 2637-2642. doi: 10.1182 / bloodadvances.2017011536
- 4. Oldenburg J., Schwaab R., Brackmann HH (1999) Induction of immune tolerance in haemophilia A inhibitor patients by the ‘Bonn Protocol «: predictive parameter for therapy duration and outcome. Vox Sang., 77 (Suppl. 1): 49-54. doi: 10.1159 / 000056717
- 5. Srivastava A., Santagostino E., Dougall A. et al. (2020) WFH Guidelines for the Managementof Hemophilia, 3rd ed. Haemophilia, 26 (Suppl. 6): 1-158. doi: 10.1111 / hae.14046
- 6. Kempton CL, Meeks SL (2014) Toward optimal therapy for inhibitors in hemophilia. Blood, 124 (23): 3365-3372. doi: 10.1182 / blood-2014-05-577643
- 7. Varadi K., Tangada S., Loeschberger M. et al. (2016) Pro- and anticoagulant factors facilitate thrombin generation and balance the haemostatic response to FEIBA (®) in prophylactic therapy. Haemophilia, 22 (4): 615-624. doi: 10.1111 / hae.12873
- 8. Antunes SV, Tangada S., Stasyshyn O. et al. (2013) Randomized comparison of prophylaxis and on-demand regimens with FEIBA NF in the treatment of haemophilia A and B with inhibitors. Haemophilia, 20 (1): 65-72. doi: 10.1111 / hae.12246
- 9. Leissinger C., Gringeri A., Antmen B. et al. (2011) Anti-inhibitor coagulant complex prophylaxis in hemophilia with inhibitors. N. Engl. J. Med., 365 (18): 1684-1692. doi: 10.1056 / NEJMoa1104435
- 10. Berntorp Е. (2009) Differential response to bypassing agents complicates treatment in patients with haemophilia and inhibitors. Haemophilia, 15 (1): 3-10. doi: 10.1111 / j.1365-2516.2008.01931.x
- 11. Leissinger C., Gringeri A., Antmen B. et al. (2011) Anti-inhibitor coagulant complex prophylaxis in hemophilia with inhibitors. N. Engl. J. Med., 365 (18): 1684-1692.
- 12. Collins PW, Chalmers E., Hart DP et al. (2012) Diagnosis and treatment of factor VIII and IX inhibitors in congenital haemophilia, 4th ed. Brit. J. Haematol., 160 (Iss. 2). https://doi.org/10.1111/bjh.12091
- 13. Zozulya NI, Kumskova MA, Polyanskaya T.Yu, Svirin PV (2018) Clinical practice guidelines for the diagnosis and treatment of hemophilia. Moscow. (In Rus.).
|
Сведения об авторе: Стасишин Александра Васильевна — доктор медицинских наук, ведущий научный сотрудник ГУ «Институт патологии крови и трансфузионной медицины АМН Украины», Украина. ORCID ID: 0000-0002-8366-5926 Адрес для корреспонденции: Стасишин Александра Васильевна |
Information about the author: Stasyshyn Oleksandra V. — Doctor of Medical Sciences, Leading researcher of SI «Institute of blood pathology and transfusion medicine of NAMS of Ukraine», Lviv, Ukraine. ORCID ID: 0000-0002-8366-5926 Address for correspondence: Oleksandra Stasyshyn |
Поступила в редакцию / Received: 25.01.2021
Принято к печати / Accepted: 09.02.2021
пройти тест
.
[ad_2]