Резюме. Эффективность и безопасность биосимилярив в лечении взрослых с атопическим дерматитом
актуальность
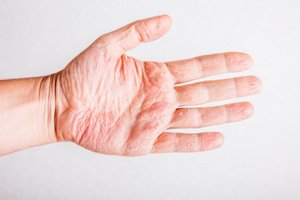
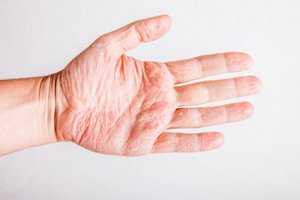 Атопический дерматит (АД) — хроническое заболевание кожи, одно из триады аллергических болезней, дебют которого приходится на период раннего детства. Однако, согласно статистическим данным, до 10% пациентов заболевают АД во взрослом возрасте (Silverberg JI, Hanifin JM, 2013). Особенностями клинической характеристики взрослых с АД является длительное течение и многочисленные обострения, при которых возникает зуд кожи различной степени выраженности, больше всего — в ночное время на боковых поверхностях тела, сгибах локтей и коленей, лице, веках. В современных взглядах на механизм формирования нарушения большое внимание уделяют возникновению неспецифического воспаления. Считается, что связаны между собой стимулирующие факторы и факторы АД приводят к активации иммунокомпетентных клеток и повышение выработки провоспалительных цитокинов, в частности интерлейкина-2 и -4. В результате фенотип антигенпрезентуючих клеток превращается в воспалительный фенотип и формируются аллергенспецифических Т- и В-лимфоциты, которые поражают органы-мишени, в частности кожу. Несмотря на имеющиеся возможности медикаментозного лечения, в части взрослых пациентов с АД длительно сохраняются остаточные клинические симптомы, значительно ухудшает качество жизни и приводит к негативным социальным последствиям. Предыдущие исследования свидетельствовали об удовлетворительной клинический ответ на применение рекомбинантного антитела IgG дупилумабу (Hendricks AJ et al., 2019). Однако инъекционная форма выпуска препарата и серьезные побочные эффекты от длительного применения вызвали дальнейший поиск эффективного таргетной лекарственного средства, один из которых — низкомолекулярный биосимиляр аброцитиниб, механизм действия которого заключается в блокировании фермента янус киназы-1 и последовательном уменьшении выработки интерлейкцну-4. Группа исследователей отделения дерматологии Вашингтонского университета во главе с Джонатаном Сильвербергом (Silverberg J. et al., 2020) исследовали дозозависимый лечебный эффект и безопасность аброцитинибу (NCT03575871). Результаты опубликованы в журнале JAMA Dermatology ( «Дерматология» Американской медицинской ассоциации).
Атопический дерматит (АД) — хроническое заболевание кожи, одно из триады аллергических болезней, дебют которого приходится на период раннего детства. Однако, согласно статистическим данным, до 10% пациентов заболевают АД во взрослом возрасте (Silverberg JI, Hanifin JM, 2013). Особенностями клинической характеристики взрослых с АД является длительное течение и многочисленные обострения, при которых возникает зуд кожи различной степени выраженности, больше всего — в ночное время на боковых поверхностях тела, сгибах локтей и коленей, лице, веках. В современных взглядах на механизм формирования нарушения большое внимание уделяют возникновению неспецифического воспаления. Считается, что связаны между собой стимулирующие факторы и факторы АД приводят к активации иммунокомпетентных клеток и повышение выработки провоспалительных цитокинов, в частности интерлейкина-2 и -4. В результате фенотип антигенпрезентуючих клеток превращается в воспалительный фенотип и формируются аллергенспецифических Т- и В-лимфоциты, которые поражают органы-мишени, в частности кожу. Несмотря на имеющиеся возможности медикаментозного лечения, в части взрослых пациентов с АД длительно сохраняются остаточные клинические симптомы, значительно ухудшает качество жизни и приводит к негативным социальным последствиям. Предыдущие исследования свидетельствовали об удовлетворительной клинический ответ на применение рекомбинантного антитела IgG дупилумабу (Hendricks AJ et al., 2019). Однако инъекционная форма выпуска препарата и серьезные побочные эффекты от длительного применения вызвали дальнейший поиск эффективного таргетной лекарственного средства, один из которых — низкомолекулярный биосимиляр аброцитиниб, механизм действия которого заключается в блокировании фермента янус киназы-1 и последовательном уменьшении выработки интерлейкцну-4. Группа исследователей отделения дерматологии Вашингтонского университета во главе с Джонатаном Сильвербергом (Silverberg J. et al., 2020) исследовали дозозависимый лечебный эффект и безопасность аброцитинибу (NCT03575871). Результаты опубликованы в журнале JAMA Dermatology ( «Дерматология» Американской медицинской ассоциации).
результаты
К исследованию привлечены 391 пациент в возрасте ˃ 12 лет с умеренным или тяжелым субклиническим течением дерматита на фоне применения стандартизированного лечения ˂4 нед за последние 6 мес. Две интервенционные группы получали аброцитиниб в дозе 100 и 200 мг (155 и 158 пациентов). Третья группа была контрольной (78 пациентов). По результатам опроса по шкале общей оценки исследователя (EASI-75) определяли минимальное площади повреждения кожи и тяжести экземы на 12-й неделе (≥75% точек шкалы). По вторичную точку исследования было выбрано удельную долю пациентов, достигших улучшения ≥4 точек с многочисленной рейтинговой шкале максимального зуд (PP-NRS). Дополнительно исследовали безопасность препарата и лабораторные показатели.
- В общем получены достоверные статистические данные лечебной эффективности аброцитинибу в интервенционных группах по сравнению с контрольной (р˂0,001). В частности, в группе аброцитинибу 100 мг улучшение по шкале EASI-75 обнаружили в 28,4% пациентов в группе аброцитинибу 200 мг — в 38,1%, тогда как в контрольной группе улучшение наблюдалось в 10,4% пациентов. Углубленное опроса по шкале EASI-90 тоже свидетельствует о клинической ответ пациентов интервенционных групп по сравнению с контрольной группой (23,9 и 37,7 vs 3,9% соответственно, р˂0,001).
- Зуд уменьшилось не менее чем на 4 точки по шкале PP-NRS в 45,2% пациентов группы аброцитинибу 100 мг и в 55,3% пациентов группы аброцитинибу 200 мг, тогда как в контрольной группе уменьшения зуда определялось только в 11,5% пациентов (р˂ 0,001).
- Частота нежелательных явлений оказалась зависимой от дозы препарата и была самой у пациентов группы 200 мг (65,8%), а самой низкой — в контрольной группе (53,8%). Однако самую высокую частоту серьезных побочных эффектов выявлено в группе аброцитинибу 100 мг (3,2% пациентов) по сравнению с группой аброцитинибу 200 мг (1,3% пациентов) и контрольной (1,3% пациентов).
- В 1,3% пациентов группы аброцитинибу 200 мг отмечалась тромбоцитопения, которая не нуждалась фармакологической коррекции.
выводы
Таким образом, необходимы дальнейшие исследования с целью поиска путей стандартизации применения низкомолекулярных биосимилярив у пациентов с атопическим дерматитом.
- Silverbreg J., Simpson E., Thyssen J. (2020) Efficacy and Safety of Abrocitinib in Patients With Moderate-to-Severe Atopic DermatitisA Randomized Clinical Trial. JAMA Dermatol., 156 (8): 863-873. doi: 10.1001 / jamadermatol.2020.1406.
- Silverberg JI, Hanifin JM (2013) Adult eczema prevalence and associations with asthma and other health and demographic factors: a US population-based study. J. Allergy Clin. Immunol., 132 (5): 1132-1138. doi: 10.1016 / j.jaci.2013.08.031PubMedGoogle Scholar
- Hendricks AJ, Lio PA, Shi VY (2019) Management recommendations for dupilumab partial and non-durable responders in atopic dermatitis. Am. J. Clin. Dermatol., 20 (4): 565-569. doi: 10.1007 / s40257-019-00436-8PubMedGoogle Scholar
- По материалам www.jamanetwork.com/journals/jamadermatology/fullarticle/2766772
Жарикова Юлия
.
[ad_2]