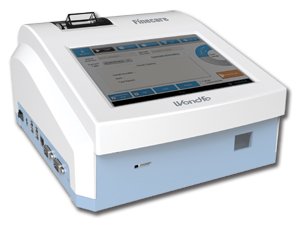
Резюме. Лабораторные тест-системы для проведения количественного экспресс-анализа с применением иммунофлуоресцентного метода на основе тест-полосок находят все большее клиническое применение. Использование «сухого» метода химического анализа позволило максимально упростить процедуру и получить анализы экспертного уровня качества. Приведенное в полной мере касается анализатора «FinecareTM FIA Meter » ( «Wondfo®», Китай). Актуальность этих приборов особенно ощутима во время пандемии COVID-19.
УДК 578.834: 57.083.3
DOI: 10.32471 / umj.1680-3051.141.199518
 По данным Всемирной организации здравоохранения, по состоянию на 03.02.2021 г.. Во всем мире зарегистрировано 103 362 039 подтвержденных случаев COVID-19, который привел к 2244713 смертей [1]. Среди причин летального исхода — тяжелая бактериальная пневмония, острый респираторный дистресс-синдром с полиорганной недостаточностью, развитие тромбоэмболических осложнений, которые обычно вызываются нарушением коагуляционной способности системы гемостаза на фоне активации гиперкоагуляции и повышенной тромбогенности крови [2–5]. У больных с тяжелым течением COVID-19 проявляют значительно более высокие уровни С-реактивного белка (СРБ), прокальцитонина (ПКТ), D-димера, сывороточного амилоида А, интерлейкина-6 и -10 по сравнению с больными с легкой и умеренной ходом [6]. Указанные показатели имеют прямая корреляционная связь с ухудшением состояния пациента и прогнозируют высокую вероятность летального исхода [7]. Именно поэтому каждый из этих показателей сегодня рассматривается как предвестник развития угрожающих состояний, и одновременно является надежным маркером для контроля лечебных мероприятий.
По данным Всемирной организации здравоохранения, по состоянию на 03.02.2021 г.. Во всем мире зарегистрировано 103 362 039 подтвержденных случаев COVID-19, который привел к 2244713 смертей [1]. Среди причин летального исхода — тяжелая бактериальная пневмония, острый респираторный дистресс-синдром с полиорганной недостаточностью, развитие тромбоэмболических осложнений, которые обычно вызываются нарушением коагуляционной способности системы гемостаза на фоне активации гиперкоагуляции и повышенной тромбогенности крови [2–5]. У больных с тяжелым течением COVID-19 проявляют значительно более высокие уровни С-реактивного белка (СРБ), прокальцитонина (ПКТ), D-димера, сывороточного амилоида А, интерлейкина-6 и -10 по сравнению с больными с легкой и умеренной ходом [6]. Указанные показатели имеют прямая корреляционная связь с ухудшением состояния пациента и прогнозируют высокую вероятность летального исхода [7]. Именно поэтому каждый из этих показателей сегодня рассматривается как предвестник развития угрожающих состояний, и одновременно является надежным маркером для контроля лечебных мероприятий.
Так,> 7-кратное повышение уровня D-димера у больных с тяжелым течением COVID-19 на фоне роста концентрации фибриногена и увеличение протромбинового времени и тромбоцитопении послужило предвестником повышения летальности почти вдвое [8–10]. Его повышение ассоциированное с ростом частоты угрожающих тромбоэмболических осложнений, особенно у пациентов с тромбофилией или тромботических прошлым в анамнезе [11]. Важным предвестником ожидаемого тяжелого состояния или ухудшение течения заболевания равны острофазовые белков — СРБ и ПКТ. Их повышенная концентрация в крови, наблюдается в ближайшие времена острого воспалительного процесса, довольно надежным прогностическим фактором. Их диагностическая ценность особенно ощутима в случае прогнозирования развития таких тяжелых состояний, как сепсис, полиорганная недостаточность и цитокиновый шторм [12]. Последний является важным звеном патогенетической развития ухудшения клинического состояния больных COVID-19. Так, клинико-лабораторная оценка концентрации ПКТ с учетом клинического состояния больного при острых респираторных вирусных инфекциях, в частности при COVID-19, может иметь решающее значение для своевременного назначения и продолжительности антибактериальной терапии [13, 14].
Сегодня методы лабораторного определения тех или иных биохимических / химических маркеров, которые доказывали бы развитие угрожающих нарушений в организме больного и вероятность развития негативных событий, стали неотъемлемой частью стратификации рисков лечебному процессу. Особенно актуальным вопрос качественной и своевременной лабораторной диагностики встал во время пандемии COVID-19. Такие показатели, как D-димер и ПКТ — среди обязательных тестов у пациентов с COVID-19 [15]. Однако их массовое внедрение без современных технологических решений маловероятно. Помочь этому могут современные приборы, которые обеспечивают миниатюризацию процессов анализа с сохранением надежности и информативности их результатов. Обычно для этого используют:
- тест-полоски (метод «сухой химии»);
- картриджи, слайды (метод иммунохроматографии)
- биосенсоры — токопроводящих полоски (метод потенциометрии)
- латексные тест-системы.
Приборы на основе указанных технологий не требуют для обслуживания высококвалифицированного персонала и позволяют проводить лабораторные исследования обученным медицинским персоналом непосредственно у постели больного (англ. point-of-care testing). Это позволяет максимально сократить время проведения исследования и получения ответа на поставленный клиническое задачи, упростить процедуру проведения исследования и сделать ее доступной для медицинского персонала без специальной аналитической образования. Большинство устройств позволяет получить визуальную информацию результатов тестирования мгновенно, что стало решающим в выборе сферы их применения: отделение неотложной помощи и кареты скорой помощи, палаты интенсивной терапии лечебных учреждений общего профиля, кабинеты семейного врача и для личного домашнего применения. Приведенные аргументы способствовали стремительному распространению портативных клинических анализаторов среди медицинских учреждений.
Среди приборов, которые нашли широкое клиническое применение, в частности в Украине, — лабораторное оборудование компании «Wondfo®»(Китай) — система «FinecareTM FIA Meter » для проведения количественного экспресс-анализа с применением иммунофлуоресцентного метода (на основе использования тест-полосок для «сухого» химического анализа). Система способна помочь в диагностике таких состояний, как воспаление, сепсис, сахарный диабет, сердечно-сосудистые заболевания, поражения почек, онкологические заболевания и тому подобное. Анализатор позволяет провести исследования крови и мочи в течение нескольких минут за 36 показателям, среди которых:
- тесты на воспаление (ПКТ, СРБ, сывороточный амилоид А)
- маркер коагуляции D-димер;
- кардиомаркеры (мозговой натрийуретический пептид, тропонин I и др.)
- гликозилированный гемоглобин;
- маркеры поражения почек (микроальбумин, цистатин-С, ренальный тропонин, β2-микроглобулин)
- орионичний гонадотропин;
- широкий спектр гормонов (12 показателей);
- витамин D.
Клиническое применение указанного прибора может обеспечить тщательный контроль лечебного процесса на всех этапах: от момента госпитализации до выписки и амбулаторного наблюдения.
Список литературы / References:
- 1. WHO (2021) WHO Coronavirus Disease (COVID-19) Dashboard (https://covid19.who.int/).
- 2. Wichmann D., Sperhake J.-P., Lütgehetmann M. et al. (2020) Autopsy Findings and Venous Thromboembolism in Patients With COVID-19. Ann. Intern. Med. doi: 10.7326 / M20-2003.
- 3. Helms J., Tacquard C., Severac F. et al. (2020) High risk of thrombosis in patients with severe SARS-CoV-2 infection: a multicenter prospective cohort study. Intensive Care Med. doi: 10.1007 / s00134-020-06062-x.
- 4. Corrêa TD, Cordioli RL, Guerra JCC et.al. (2020) Coagulation profile of COVID-19 patients admitted to the ICU: An exploratory study. PLoS One, 15 (12): e0243604. doi: 10.1371 / journal.pone.0243604.
- 5. Klok FA, Kruip M., van der Meer NJM et al. (2020) Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb. Res., 191: 145-147. doi: 10.1016 / j.thromres.2020.04.013.
- 6. Осадчий А.И. (2021) COVID-19 повышает риск тромбозов. Укр. мед. журнал (https://www.umj.com.ua/article/197100).
- 7. Silva TF, Pellissier FT, Sanfelice RA et al. (2020) A 21st Century Evil: Immunopathology and New Therapies of COVID-19. Front. Immunol., 11: 562264. doi: 10.3389 / fimmu.2020.562264.
- 8. Lippi G., Plebani M., Henry BM (2020) Thrombocytopenia is associated with severe coronavirus disease 2019 (COVID-19) infections: a meta-analysis. Clin. Chim. Acta, 506: 145-148. doi: 10.1016 / j.cca.2020.03.022.
- 9. Iba T., Levy JH, Connors JM et al. (2020) The unique characteristics of COVID-19 coagulopathy. Crit. Care, 24: 360 doi: 10.1186 / s13054-020-03077-0.
- 10. Ribes A., Vardon-Bounes F., Mémier V. et al. (2020) Thromboembolic events and Covid-19. Adv. Biol. Regul., 77: 100735. doi: 10.1016 / j.jbior.2020.100735.
- 11. Wichmann D., Sperhake J.-P., Lütgehetmann M. et. al. (2020) Autopsy Findings and Venous Thromboembolism in Patients With COVID-19. Ann. Intern. Med., 15 (https://doi.org/10.7326/M20-2003).
- 12. Creamer AW, Kent AE, Albur M. (2019) Procalcitonin in respiratory disease: use as a biomarker for diagnosis and guiding antibiotic therapy. Breathe, 15: 296-304. doi: 10.1183 / 20734735.0258-2019.
- 13. Sims CR, Nguyen TC, Mayeux PR (2016) Could Biomarkers Direct Therapy for the Septic Patient? J. Pharmacol. Exp. Ther., 357 (2): 228-239. doi: 10.1124 / jpet.115.230797.
- 14. Kahn RE (2009) Procalcitonin to guide duration of antibiotic therapy in intensive care patients: some research questions. Crit. Care, 13 (4): 414.
- 15. Министерство здравоохранения Украины (2020) Приказ МЗ Украины от 21.07.2020 г.. № 1653 «О внесении изменений в протокол« Оказание медицинской помощи для лечения коронавирусной болезни (COVID-19) ».
.
[ad_2]