DOI: 10.32471 / umj.1680-3051.141.197975
УДК 616.151.5
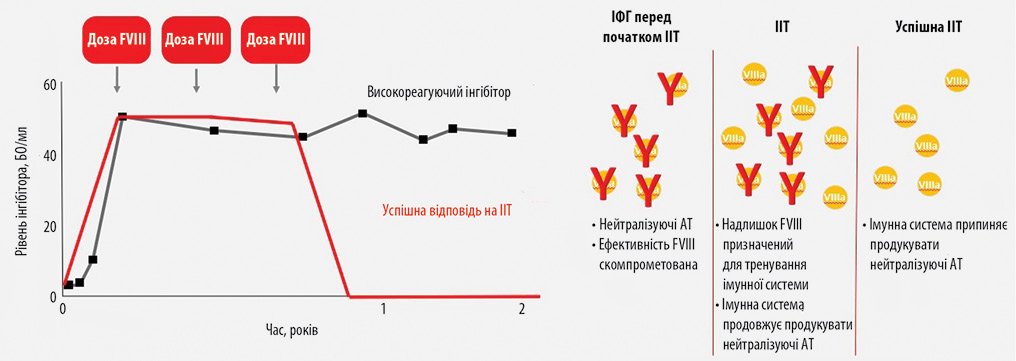
Сегодня развитие ингибиторной формы гемофилии (ИФГ) — одна из самых больших проблем в лечении пациентов с гемофилией. Выведение ингибиторов путем проведения терапии по методу индукции иммунной толерантности (ИИТ) — первая линия терапии у пациентов с ингибитором. Этот метод заключается в частом назначении высоких доз концентрата фактора свертывания, чтобы приучить организм принимать лечение без реакции на него [1, 2]. Большинство больных становятся толерантными в течение 12 мес, но в более резистентных случаях может потребоваться ≥2 лет (рис. 1). Традиционный подход ИИТ при менеджменте пациентов с ИФГ заключается в том, что перед проведением ИИТ необходимо ждать <2 лет до снижения титра ингибитора <10 БУ, при отсутствии тяжелых кровотечений у пациента. Однако результаты исследования A. Rocino и соавторов (2016) показали, что, во-первых, время до начала ИИТ важнее, чем величина самого титра в начале ИИТ, и, во-вторых, отсутствие связи между титром ингибитора и началом ИИТ [3]. Полученные результаты опровергли эффективность традиционного подхода к ИИТ. В 2017 обнародованы рекомендации Организации врачей Центра гемофилии Великобритании (The United Kingdom Haemophilia Centre Doctors 'Organisation - UKHCDO) по менеджмента пациентов с гемофилией, в которых указано, что, согласно современному подходу, ИИТ рекомендуется начинать как можно быстрее, независимо от титра ингибитора (рис. 2) [4].
Рисунок 1. Успешная ИИТ
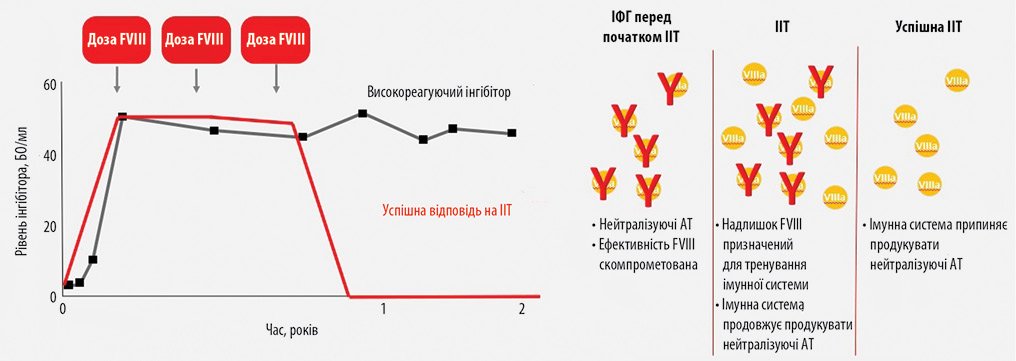
БУ — Бетезда единицы; АО — антитела.
Рисунок 2. Алгоритм эрадикации ингибитора путем ИИТ
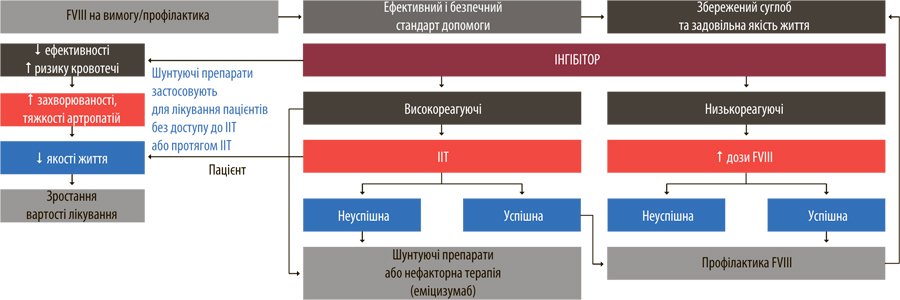
Возможности элиминации ингибитора изучают на протяжении многих лет. Сегодня имеющиеся несколько протоколов терапии (табл. 1). Общему мнению по вопросу оптимальной дозировки и частоты доз при ИИТ не существует; сейчас проводятся международные исследования, чтобы сравнить результаты применения 50 МЕ и 200 МЕ. Данные литературы свидетельствуют, что наибольшее распространение получили две схемы ИИТ: низко- и высокодозной протоколы, но данные предыдущих исследований относительную эффективность этих схем достаточно противоречивы, что связано с тем, что в исследованиях применяли различные критерии эффективности, рассматриваемые группы были эквивалентными и использовали различные подходы к терапии. Кроме того, при анализе результатов эффективности протоколов ИИТ важно учитывать факторы, влияющие на ее эффективность.
Таблица 1. ИИТ-протоколы терапии при гемофилии А
|
ИИТ-протоколы терапии при гемофилии А |
|
|
протокол |
доза |
|
Боннский протокол / высокодозной |
100-150 МЕ FVIII / кг каждые 12 ч Сопутствующее лечение с применением препаратов из шунтирующих механизмом действия (АРСС или rFVIIa раза в сутки), в соответствии с тенденцией кровотечений |
|
высокодозной |
200 МЕ FVIII / кг каждые 24 ч |
|
Середньодозовий |
100 МЕ FVIII / кг ежедневно |
|
van Creveld (голландский) / низкодозовый |
25-50 МО FVIII / кг через день |
АРСС — антиингибиторний коагуляционный комплекс; rFVIIa — рекомбинантный активированный FVII.
Таблица 2. Варианты возможных результатов ИИТ
|
результаты ИИТ |
|
|
эффективность |
значение показателя |
|
успешная ИИТ |
Критерии успешной ИИТ:
|
|
Частичный успех ИИТ |
Имеющиеся 2 с 3 критериев успешной ИИТ |
|
частичный ответ |
Имеющийся 1 с 3 критериев успешной ИИТ |
|
отсутствует ответ |
Нет ни одного из критериев успешной ИИТ течение ≥12 мес |
Факторы, влияющие на результат ИИТ:
- Общепринятые факторы успешной ИИТ:
— исторический пик титра ингибитора <200 БУ;
— титр ингибитора на момент начала ИИТ <10 БУ.
- Косвенные факторы успешной ИИТ:
— начало в возрасте <6 лет
— начало в течение 2 лет с момента развития ингибитора.
- Неблагоприятный фактор проведения ИИТ:
— повышение титра ингибитора> 500 БУ после начала ИИТ.
С учетом этих факторов, данные исследования CE Ettingshausen и W. Kreuz (2013) позволили сделать вывод, что у пациентов с прогностическими факторами успешной ИИТ имеющийся положительный результат по элиминации ингибитора, независимо от выбранного протокола [5]. Также выявлено, что низкодозовый протокол ИИТ более длительным по времени и имеет высокую частоту геморрагических эпизодов по сравнению с высокодозной протоколом. Эти выводы свидетельствуют в пользу того, что у пациентов с неблагоприятными прогностическими факторами преимущество должно отдаваться высокодозной протокола ИИТ.
Рекомендации по мониторингу титра ингибитора в ходе ИИТ:
- в начале ИИТ титр ингибитора необходимо определять еженедельно для выявления пика ингибитора, затем — ежемесячно для оценки ответа на ИИТ;
- при анализе Бетезда в модификации Ниймеген не использовать период отмывки;
- снижение титра ингибитора как минимум на 20% каждые 6 мес после достижения пика свидетельствует о развитии толерантности и не требует изменений в терапии
- после снижения титра ингибитора <0,6 БО / мл определение титра ингибитора следует повторять каждые 3 мес в период до 2 лет после окончания ИИТ, затем - ежегодно.
Рекомендации по мониторингу титра ингибитора после окончания ИИТ:
- мониторинг ингибитора в тесте Бетезда и определения остаточной активности FVIII проводится ежемесячно в течение 6 мес, затем — каждые 2 мес в течение года, затем в рутинном порядке;
- при рецидиве ингибитора рекомендуется немедленное восстановление ИИТ.
Согласно современным рекомендациям, ИИТ считают успешной тогда, когда достигнуты следующие показатели: персистирующий титр ингибитора <0,6 БО / мл, активность восстановление FVIII ≥66%, период полувыведения FVIII ≥6 ч у взрослых и ≥7 ч у детей. Решение об остановке ИИТ должно быть принято, когда титр ингибитора не повышался ≥20% в пределах 9 мес от начала лечения достигнута хотя бы частичный ответ на лечение в пределах 33 мес [6, 7] (Табл. 2).
Таким образом, ИИТ — первая линия терапии у пациентов с ИФГ, которая обеспечивает элиминацию ингибитора. Однако, несмотря на эффективность ИИТ, этот метод демонстрирует неэффективность в 30% случаев. Кроме того, ИИТ связана с рядом недостатков, включая потребности в постоянном венозном доступе и инфекциями, ассоциированными со средствами центрального венозного доступа, приверженностью пациентов к лечению и доступности препарата фактора свертывания. Последнее обусловило недостаточное применение ИИТ в большинстве стран, в том числе и в Украине, что связано с недостаточным обеспечением факторами свертывания крови на душу населения. По данным общественной организации инвалидов «Всероссийское общество гемофилии», до 2017 г.. Уровень обеспечения VIII фактором свертывания крови в Украине составил 0,8 Ед. / Год на душу населения, тогда как, согласно нормам Всемирной федерации гемофилии (World Federation of Hemophilia — WFH), для обеспечения выживаемости пациентов с гемофилией необходимо уровень не ниже 1 Ед. / год. Соответственно, при невозможности проведения или неэффективности ИИТ, профилактику кровотечений рекомендуется проводить препаратом нефакторных терапии (емицизумаб) или препаратами с шунтирующих механизмом действия, такими как АРСС или rFVIIa, в частности как сопровождение ИИТ [8].
При поддержке ООО «Такеда Украина»
VV-MEDMAT-37035
Список литературы / References:
- 1. Brackmann HH., White GC2nd, Berntorp E. et al. (2018) Immune tolerance induction: What have we learned over time? Haemophilia, 24 (Suppl. 3): 3-14. doi: 10.1111 / hae.13445
- 2. Bruinstroop E., Klok FA, Van De Ree MA et al. (2009) Elevated D-dimer levels predict recurrence in patients with idiopathic venous thromboembolism: a meta-analysis. J. Thromb. Haemost., 7 (4): 611-618. doi: 10.1111 / j.1538-7836.2009.03293.x
- 3. Rocino A., Cortesi PA, Scalone L. et al. (2016) Immune tolerance induction in patients with haemophilia a and inhibitors: effectiveness and cost analysis in an European Cohort (The ITER Study. Haemophilia, 22 (1): 96-102. Doi: 10.1111 / hae.12780
- 4. Collins P., Chalmers E., Alamelu J. et al. (2017) First-line immune tolerance induction for children with severe haemophilia A: A protocol from the UK Haemophilia Centre Doctors ‘Organisation Inhibitor and Paediatric Working Parties. Haemophilia, 23 (5): 654-659. doi: 10.1111 / hae.13264
- 5. Ettingshausen CE, Kreuz W. (2013) The immune tolerance induction (ITI) dose debate: does the International ITI Study provide a clearer picture? Haemophilia, 19 (Suppl. 1): 12-17. doi: 10.1111 / hae.12051
- 6. Hay CRM, DiMichele DM, International Immune Tolerance Study (2012) The principal results of the International Immune Tolerance Study: a randomized dose comparison. Blood, 119 (6): 1335-1344. doi: 10.1182 / blood-2011-08-369132
- 7. Valentino LA, Kempton CL, Kruse-Jarres R. et al. (2015) US Guidelines for immune tolerance induction in patients with haemophilia a and inhibitors. Haemophilia, 21 (5): 559-567. doi: 10.1111 / hae.12730
- 8. Vilchevska KV (2020) Experience of the early treatment in patients with inhibitory form of hemophilia A in conditions of limited resources. UMJ, 6 (140), V. 1: 55-58 (In Ukr.).
|
Сведения об авторе: Вильчевская Екатерина Викторовна — кандидат медицинских наук, заведующий Центром патологии гемостаза Национальной детской специализированной больницы «Охматдет», заведующий центром патологии гемостаза ГУ «Институт неотложной и восстановительной хирургии имени В.К. Гусака НАМН Украины », Киев, Украина. Адрес для корреспонденции: Вильчевская Екатерина Викторовна |
Information about the author: Vilchevska Kateryna V. — Candidate of Medical Sciences, Head of the Center of hemostasis pathology of the National Children Special Hospital «Ohmatdet», Head of the Center of hemostasis pathology of the VK Gusak Institute of Urgent and Recovery Surgery of NAMS of Ukraine, Kyiv , Ukraine. Address for correspondence: Kateryna Vilchevska |
Поступила в редакцию / Received: 19.01.2021
Принято к печати / Accepted: 27.01.2021
пройти тест
.
[ad_2]