13 Ноя COVID-19 и декомпенсированный цирроз печени
Резюме. Обсуждаются проблемы наблюдения пациентов с прогрессирующим заболеванием печени во время пандемии COVID-19.
Актуальность и результаты
 Учитывая иммунную дисфункцию и чрезвычайно высокую частоту коморбидности, пациентов с прогрессирующим заболеванием печени (ПЗУ) относят к группе повышенного риска осложненного течения SARS-CoV-2 (Fix OK et al., 2020). Установлены особенности распространения в популяции и высокая вирулентность коронавируса требуют соблюдения определенных мер — от незначительных ограничений к строгому карантина. Однако эпидемиологические мероприятия существенно ограничили доступность квалифицированной медицинской помощи пациентам с ПЗУ, что обусловило пересмотр лечебной стратегии и смещение акцента с агрессивным методам лечения на рутинное наблюдения этих пациентов. Отсутствие достаточного качественного опыта лечения и мониторинга пациентов с ПЗУ в карантинных условиях побудило ведущих экспертов — гепатологов мирового уровня Рассела Розенблатта (Rosenblatt R.) и Элизабет Верна (Verna E.), Центр лечения заболеваний печени и трансплантации., Г. Нью-Йорк, США, провести анализ имеющихся проблем (Verna EC, Rosenblatt R., 2020) с целью дополнения действующих рекомендаций. Основная цель исследования — установление новых клинических характеристик пациентов с некомпенсированным циррозом. Результаты опубликованы в журнале «Clinical Liver Disease» (Патология печени).
Учитывая иммунную дисфункцию и чрезвычайно высокую частоту коморбидности, пациентов с прогрессирующим заболеванием печени (ПЗУ) относят к группе повышенного риска осложненного течения SARS-CoV-2 (Fix OK et al., 2020). Установлены особенности распространения в популяции и высокая вирулентность коронавируса требуют соблюдения определенных мер — от незначительных ограничений к строгому карантина. Однако эпидемиологические мероприятия существенно ограничили доступность квалифицированной медицинской помощи пациентам с ПЗУ, что обусловило пересмотр лечебной стратегии и смещение акцента с агрессивным методам лечения на рутинное наблюдения этих пациентов. Отсутствие достаточного качественного опыта лечения и мониторинга пациентов с ПЗУ в карантинных условиях побудило ведущих экспертов — гепатологов мирового уровня Рассела Розенблатта (Rosenblatt R.) и Элизабет Верна (Verna E.), Центр лечения заболеваний печени и трансплантации., Г. Нью-Йорк, США, провести анализ имеющихся проблем (Verna EC, Rosenblatt R., 2020) с целью дополнения действующих рекомендаций. Основная цель исследования — установление новых клинических характеристик пациентов с некомпенсированным циррозом. Результаты опубликованы в журнале «Clinical Liver Disease» (Патология печени).
Варикозное расширение вен пищевода
1. Согласно действующим клиническими установками, эзофагогастродуоденоскопия (ЭГДС) — метод первой линии для проведения скрининга и лечения варикозного расширения вен пищевода у пациентов с некомпенсированным циррозом печени. Учитывая эпидемиологические ограничения, принятие решения об отсрочке процедуры основывают на показателях ригидности печени <20-25 кПа отдельно или в комбинации с тромбоцитами периферической крови> 150 000 / мм3 (Garcia-Tsao G. et al., 2017).
2. Экспертами рекомендовано расширение применения неселективных блокаторов β-адренорецепторов, исходя из показателя ригидности печени <20-25 кПа и численности тромбоцитов (Tr)> 150000 / мм3.
3. Абсолютными показаниями для выполнения ЭГДС остаются острое кровотечение из пищевода и процедура последовательного перевязки варикозных пищеводных вен.
Экспертами предложен такой алгоритм (схема 1).
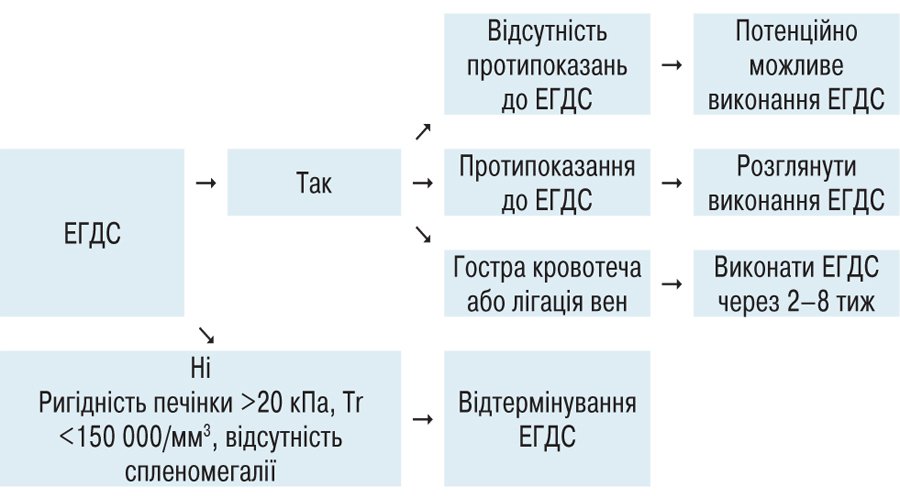
Схема 1. Алгоритм принятия клинически правильного решения
гепатоцеллюлярной карцинома
1. В отличие от постоянных рекомендаций рутинного проведения скрининга гепатоцеллюлярной карциномы (ГЦК) каждые 6 мес, после определения факторов риска рекомендуется снизить частоту скрининга до 1 раза в 8 мес, поскольку определенное время удвоения опухолевой массы составляет 4-8 мес (Meyer T. et al., 2020).
2. Решение о интервалов посещения специалиста при подозрении на ГЦК или наблюдением за стадийностью заболевания принимается многопрофильной командой специалистов с учетом наличия специалистов в медицинском учреждении, нагрузка на технический ресурс и определения степени комфорта медицинского персонала и пациента (схема 2).
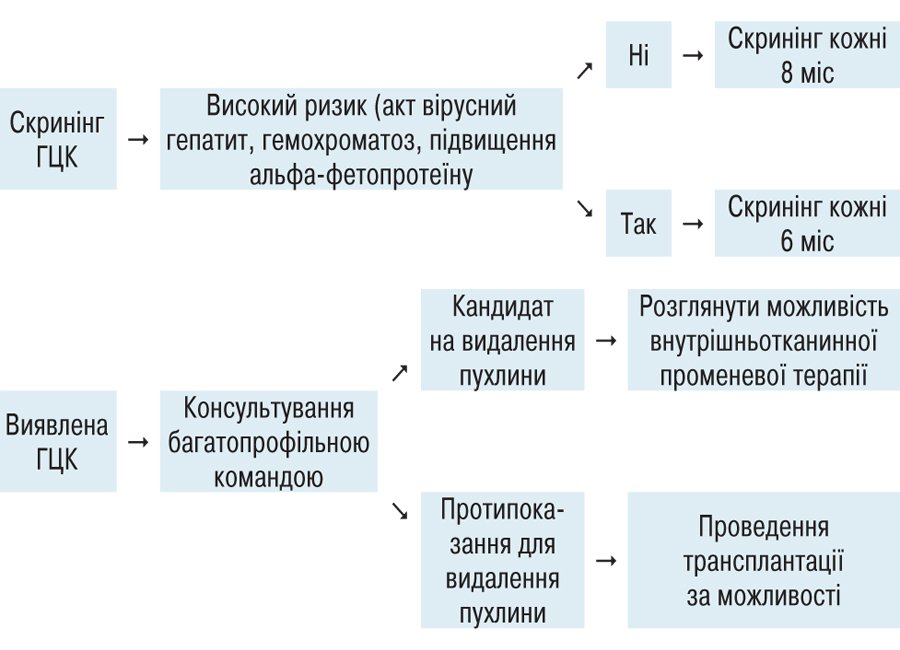
Схема 2. Простой алгоритм принятия решения
Мониторинг пациентов до / после трансплантации печени
1. В современных взглядах на механизм коронавирусной инфекции внимание уделяется чрезмерной иммунном ответе, которая вызывает высокую смертность среди группы риска, в которую входят пациенты с ПЗУ. -Прежнему имеется недостаток результатов выживаемости пациентов, перенесших трансплантацию органов, во время пандемии респираторной инфекции. Согласно статистическим данным, в США смертность среди этих пациентов достигает 24%, с повышением до 52% в случае применения респираторной поддержки.
2. Вопросы применения препаратов с иммуносупрессивной действием остается спорным. Анализ летальности у пациентов с ПЗУ в Италии не свидетельствует о дозозависимый влияние иммуносупрессоров на летальность пациентов с некомпенсированным циррозом печени.
3. Безопасность применения антивирусных и иммуномодулирующих препаратов требует дальнейшего исследования. Решение по применению препаратов патогенетического лечения принимается многопрофильной командой по принципу преимущества пользы над риском в каждом отдельном случае в зависимости от клинических симптомов и коморбидности.
4. С целью уменьшения размера опухоли у пациентов с ПЗУ предпочтение отдается методам местно-регионарной терапии, радиоемболизации иттрием 90 (90Y).
5. Также остается невыясненным продолжительность приобретенного иммунитета против респираторной инфекции, вызванной новым штаммом коронавируса, что требует поиска новых подходов к подготовке и проведению трансплантации печени.
Таким образом, необходимо проводить исследования дополнительных факторов риска, которые повышают вероятность осложненного течения SARS-CoV-2 у пациентов с ПЗУ.
- Garcia-Tsao G., Abraldes JG, Berzigotti A. et al. (2017) AASLD practice guidelines: portal hypertensive bleeding in cirrhosis: risk stratification, diagnosis, and management. Hepatology, 65: 310-335.
- Fix OK, Hameed B., Fontana RJ et al. (2020) Clinical Best Practice Advice for Hepatology and Liver Transplant Providers During the COVID-19 Pandemic: AASLD Expert Panel Consensus Statement. Hepatology. Available at: 10.1002 / hep.31281.
- Meyer T., Chan S., Park J. (2020) Management of HCC during COVID-19: ILCA guidance. Apr. 8 (https://ilca-online.org/management-of-hcc-during-covid-19-ilca-guidance/).
- Verna EC, Rosenblatt R. (2020) COVID 19: Management of Decompensated Cirrhosis and Liver Transplant Recipients. Clin. Liver Dis. (Hoboken), 15 (5): 200-203. Published online 2020 May 21 doi: 10.1002 / cld.968 (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7280636/).
Юлия Жарикова
.
[ad_2]


