
17 Июн НАЖХП от стеатоза к циррозу печени
Резюме. 8 июня в цифровом формате при содействии Украинской ассоциации метаболической медицины состоялся вебинар «Неалкогольная жировая болезнь печени (НАЖХП) и коморбидные заболевания. Опасное сочетание ». В рамках мероприятия Елена Бака выступила с докладом «НАЖХП от стеатоза к циррозу печени».
 8 июня в цифровом формате состоялся вебинар «Неалкогольная жировая болезнь печени и коморбидные заболевания. Опасное сочетание ». Мероприятие состоялось при содействии Украинской ассоциации метаболической медицины. В рамках вебинара Елена Бака, Заслуженный врач, научный сотрудник отдела диагностики и лечения метаболических заболеваний, заведующий гастроэнтерологического отделения ГНУ «Центр инновационных медицинских технологий» НАН Украины, выступила с докладом, в котором осветил проблему неалкогольной жировой болезни печени (НАЖХП), в частности неалкогольного стеатогепатита (НАСГ).
8 июня в цифровом формате состоялся вебинар «Неалкогольная жировая болезнь печени и коморбидные заболевания. Опасное сочетание ». Мероприятие состоялось при содействии Украинской ассоциации метаболической медицины. В рамках вебинара Елена Бака, Заслуженный врач, научный сотрудник отдела диагностики и лечения метаболических заболеваний, заведующий гастроэнтерологического отделения ГНУ «Центр инновационных медицинских технологий» НАН Украины, выступила с докладом, в котором осветил проблему неалкогольной жировой болезни печени (НАЖХП), в частности неалкогольного стеатогепатита (НАСГ).
НАСГ — самое распространенное хроническое заболевание печени, что может приводить к ухудшению качества жизни, инвалидизации и развития цирроза печени. В свою очередь, НАЖХП является более широким понятием, включающим как стеатоз печени, так и НАСГ — хронический и прогрессирующий гепатит, который развивается на фоне стеатоза печени и является крайне актуальной медико-социальной проблемой, поскольку относится к наиболее агрессивных форм НАЖХП, приводя к значительный экономический ущерб. Так, последние мировые данные свидетельствуют, что НАСГ является одним из основных заболеваний, которые приводят к трансплантации печени и связано с риском возникновения фиброза, цирроза печени и гепатоцеллюлярной карциномы (ГЦК), опередив хронический вирусный гепатит типов В и С [1].
Как известно, НАЖХП относится к печеночного проявления метаболического синдрома, соответственно, развитие этого состояния имеет ассоциации с инсулинорезистентностью, расстройствами регуляции адипонектина и оксидативного стресса у лиц с избыточной массой тела или ожирением, развивающийся вследствие высококалорийной диеты и недостаточной физической активности. Факторы, влияющие на развитие и прогрессирование НАЖХП, принято классифицировать на две группы: эндо и экзогенные. К эндогенным факторам относятся генетика и микробиота кишечника, а экзогенные включают особенности питания, употребление алкоголя и уровень физической активности (рис. 1) [2].
Факторы риска развития и прогрессирования НАЖХП / НАСГ:
- возраст ≥45 лет;
- сахарный диабет 2-го типа;
- индекс массы тела> 25 кг / м2;
- окружность талии> 94/80 см;
- артериальная гипертензия;
- ожирение;
- уровень липопротеидов низкой плотности <1 / 1,3 ммоль / л;
- тромбоцитопения и гипоальбуминемия [3].
Рисунок 1. Факторы риска и механизмы развития НАЖХП и неалкогольной ГЦК [4]
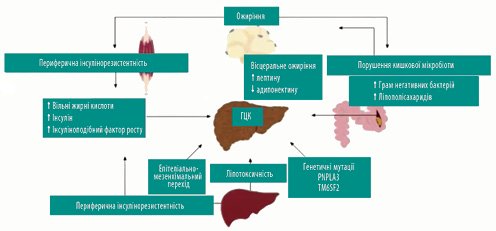
В то время как простой стеатоз при НАЖХП не коррелирует с ростом кратковременной заболеваемости и смертности, прогрессирования заболевания до НАСГ резко повышает риск развития цирроза, печеночной недостаточности и ГЦК. Современные данные свидетельствуют, что цирроз печени, ассоциированный с НАСГ — одна из ключевых причин трансплантации печени. Поскольку заболеваемость и смертность пациентов с НАСГ значительно возрастают, они еще сильнее коррелируют заболеваемостью и смертностью от сердечно-сосудистых заболеваний. Данные литературы показывают, что к основным причинам смерти, ассоциированной с НАЖХП, принадлежат не только цирроз, но и непечинковий рак, сахарный диабет и болезни легких [5]. Таким образом, инсулинорезистентность и ожирение являются основными звеньями патогенеза НАСГ, тогда как ключевыми гистологическими компонентами НАСГ является стеатоз, гепатоцеллюлярной расширения и частичное воспаление. Сегодня исследователи выделяют две основные фазы развития НАСГ: динамическая стеатотична / стеатогепатитна фаза и «нелинейная» фиброзная фаза (рис. 2).
Рисунок 2. Динамичное развитие НАСГ [6]
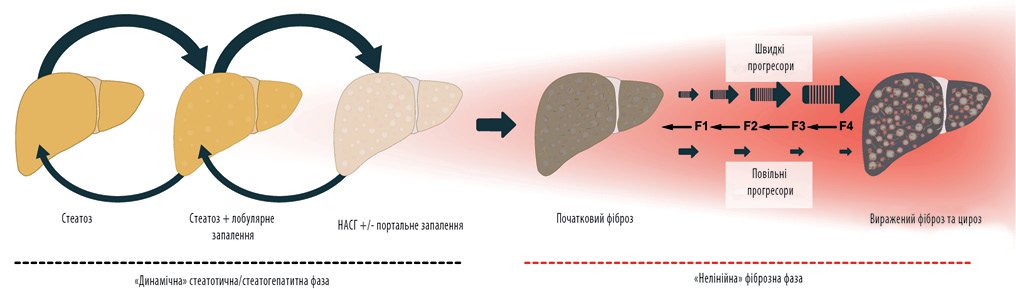
Патогенез НАСГ:
- повреждения гепатоцитов и воспаление — основные отличия НАСГ от изолированного стеатоза;
- поврежденные гепатоциты высвобождают факторы, которые обусловливают развитие воспалительного ответа, продуцируя гепатотоксичные субстанции и индуцируя дальнейшее повреждение;
- висцерального ожирения, метаболический синдром, изменения кишечной микробиоты и нарушения циркадного ритма повышают уязвимость гепатоцитов к цитокинов, кишечных метаболитов и других гепатотоксических медиаторов воспаления;
- дисрегуляция процесса регенерации может приводить к прогрессированию фиброза, цирроза и повышенного риска развития ГЦК [7].
 Учитывая тот факт, что НАСГ, в отличие НАЖХП, выражено ассоциируется с фиброзом, его диагностика базируется на проведении биопсии печени — золотом стандарте дифференциальной диагностики НАСГ и НАЖХП, и является единственным надежным методом оценки воспаления и фиброза печени (таблица). Биопсия печени обеспечивает оценку таких важных для диагностики показателей, как степень активности процесса, фиброза и исключения альтернативных диагнозов или выявления дополнительной патологии. Однако данный метод диагностики и имеет свои недостатки, включая инвазийнистю метода, осложнениями (кровотечение, гемоперитонеум, билиарный перитонит и пневмоторакс), «неточность попадания», болевые ощущения в месте прокола и высокая вариабельность в трактовке результатов [8].
Учитывая тот факт, что НАСГ, в отличие НАЖХП, выражено ассоциируется с фиброзом, его диагностика базируется на проведении биопсии печени — золотом стандарте дифференциальной диагностики НАСГ и НАЖХП, и является единственным надежным методом оценки воспаления и фиброза печени (таблица). Биопсия печени обеспечивает оценку таких важных для диагностики показателей, как степень активности процесса, фиброза и исключения альтернативных диагнозов или выявления дополнительной патологии. Однако данный метод диагностики и имеет свои недостатки, включая инвазийнистю метода, осложнениями (кровотечение, гемоперитонеум, билиарный перитонит и пневмоторакс), «неточность попадания», болевые ощущения в месте прокола и высокая вариабельность в трактовке результатов [8].
Таблица. Гистологическая картина при НАСГ и НАЖХП
| гистологическая картина | |
|---|---|
| НАЖХП | НАСГ |
| a) Изолированный стеатоз;
b) стеатоз с лобулярной или портальным воспалением без баллонной дистрофии; c) стеатоз с баллонной дистрофией, но без заполнения |
стеатоз
+ баллонная дистрофия + воспаление |
Учитывая все риски, ассоциированные с биопсией печени, в последние годы стали популярными неинвазивные методы диагностики заболеваний печени, которые базируются на двух принципах. Первый принцип — биологический, основанный на количественной оценке биомаркеров в образцах сыворотки крови. Второй принцип — физический, основанный на измерении жесткости печени. Таким образом, диагностика НАСГ базируется на определении таких диагностических критериев, как:
- повышенная активность печеночных трансаминаз;
- признаки стеатоза печени при ультразвуковом исследовании у лиц, не злоупотребляющих алкоголем;
- исключения других причин хронического гепатита (особенно вирусного гепатита В и С, аутоиммунного гепатита, гемохроматоза, болезни Вильсона — Коновалова).
В лечении НАСГ важное место отводится модификации образа жизни, которая включает обязательную диетотерапию и физическую активность, при этом предполагается умеренное уменьшение массы тела. Диетические принципы характеризуются снижением калоража на 30% или около 750-1000 ккал / сутки.
Список использованной литературы:
- 1. Younossi ZM, Golabi P., de Avila L. et al. (2019) The global epidemiology of NAFLD and NASH in patients with type 2 diabetes: A systematic review and meta-analysis. J. Hepatol .; 71 (4): 793-801. doi: 10.1016 / j.jhep.2019.06.021.
- 2. Ratziu V., Bellentani S., Cortez-Pinto H. et al. (2010) A position state-ment on NAFLD / NASH based on the EASL 2009 special conference. J. Hepatol., 53: 372-384.
- 3. Motamed N., Rabiee B., Poustchi H. et al. (2016) Non-alcoholic fatty liver disease (NAFLD) and 10-year risk of cardiovascular diseases. Clin. Res. Hepatol. Gastroenterol., 16: 30104-30108.
- 4. Cholankeril G., Patel R., Khurana S. et al. (2017) Hepatocellular carcinoma in non-alcoholic steatohepatitis: Current knowledge and implications for management. World J. Hepatol. 2017 Apr 18; 9 (11): 533-543. doi: 10.4254 / wjh.v9.i11.533.
- 5. Paik JM, Henry L., De Avila L. et al. (2019) Mortality Related to Nonalcoholic Fatty Liver Disease Is Increasing in the United States. Hepatology CommunicationsVolume 3, Issue 11: 1459-1471. doi.org/10.1002/hep4.1419.
- 6. Rinella ME, Tacke F., Sanyal AJ et al. (2019) Report on the AASLD / EASL joint workshop on clinical trial endpoints in NAFLD. Journal of Hepatology, Volume 71, Issue 4: 823-833. doi.org/10.1016/j.jhep.2019.04.019.
- 7. Neuschwander-Tetri BA (2001) A resistance movement in NASH. Am. J. Gastroenterol .; 96 (10): 2813-4. doi: 10.1111 / j.1572-0241.2001.04571.x.
- 8. Dyson JK, Anstee QM, McPherson S. (2014) Non-alcoholic fatty liver disease: a practical approach to diagnosis and staging. Frontline Gastroenterol; 5 (3): 211-218. doi: 10.1136 / flgastro-2013-100403.
.
[ad_2]


