Резюме. В статье представлены современные данные по этиологии, патогенеза, эпидемиологии и классификации вульвовагинального кандидоза. Также освещены современные международные рекомендации по лечению вульвовагинального кандидоза.
актуальность
Вульвовагинальный кандидоз (ВВК) — инфекционное поражение слизистой оболочки вульвы и влагалища, вызванное грибами рода Candida. Современные статистические данные свидетельствуют, что около 75% женщин имеют хотя бы один эпизод неосложненного ВВК в тот или иной период жизни, а 40% -> 2 эпизодов [1]. Принято считать, что основным этиологическим возбудителем ВВК на сегодня Candida albicans, Но за последние годы отмечена также тенденция к увеличению распространения ВВК, обусловленного «не-albicans» выдох, в частности C. glabrata, C. tropicalis, C. paparsilosis, C. crusei, C. lusitaniae и Saccharomyces cerevisiae, Которые, как правило, вызывают осложненное течение ВВК, который трудно поддается воздействию противогрибковых препаратов. Распространенность ВВК неодинакова в разных возрастных группах. Так, эпидемиологические исследования показывают, что чаще ВВК отмечают у женщин репродуктивного возраста (21-40 лет), то есть наиболее трудоспособная часть общества, что еще раз свидетельствует о высокой социальной значимости проблемы ВВК. У девочек до менархе и у женщин в постменопаузальный период заболевания выявляют реже. Большинство исследователей считают, что настоящая заболеваемость ВВК неизвестна из-за значительный процент самолечения [2].
Согласно современным представлениям ВВК не передается половым путем и не относится к инфекциям, передающихся половым путем, в основном расценивается как вторичная эндогенная инфекция, так как грибы рода Candida как симбиоты имеющиеся на слизистой оболочке влагалища, кроме того, они входят в состав нормальной микрофлоры рта и толстой кишки большинства здоровых людей [3]. В случае нарушения гомеостаза (снижение выработки секреторных иммуноглобулинов и влияние внешних факторов, которые вызывают увеличение численности грибов) кандидоносительства может реализоваться в развернутую инфекцию, в том числе тяжелые формы заболевания, которые сопровождаются частыми рецидивами.
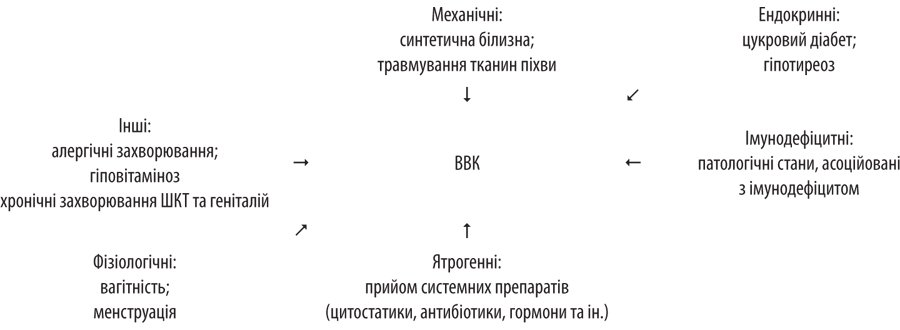
Патогенез ВВК сложный и до сих пор недостаточно изучен. Учитывая тот факт, что штаммы C. albicans, Выделенные у больных как с ВВК, так и у носителей, можно сделать вывод о ведущей роли в развитии ВВГ именно состояния макроорганизма, а не свойств возбудителя. Соответственно, ключевым триггером развития заболевания является не изменение свойств возбудителя, а снижение резистентности организма-хозяина. Причины, обусловливающие возникновение дисбиоза, принято разделять на экзо и эндогенные (рис. 1). Экзогенные факторы включают применение системных препаратов (антибиотиков, ГКС, цитостатиков, противовирусных препаратов), нерациональные спринцевания, ношение тесной одежды, белья из синтетических тканей, применение гигиенических прокладок, пороки развития половых органов, наличие инородных тел влагалища, влияние химических и физических факторов, стрессы и нерациональное питание (прием пищи с большим количеством углеводов). В свою очередь, эндогенные факторы, обусловливающие манифестацию патологического процесса, связанные в первую очередь с изменениями общего и местного иммунитета, ендокринопатиямы и изменениями гормонального статуса, которые сопровождают различные периоды жизни человека. Кроме того, эндогенными причинами ВВК также могут быть нарушения функции пищеварительного тракта и сопутствующие заболевания, в частности ожирение и сахарный диабет. Последний факт связан с тем, что грибы рода Сandida способны усиленно размножаться в углеводном среде, поэтому любые состояния, сопровождающиеся гипергликемией или гиперэстрогенией с усиленным созреванием эпителиоцитов, богатых гликогеном, создают благоприятные условия для манифестации ВВК [4].
Рисунок 1. Факторы, ассоциированные с развитием ВВК

На современном этапе принято классифицировать ВВК на две формы: острый ВВК, который характеризуется длительностью <2 мес с выраженной и типичной клинической симптоматикой, и хронический (рецидивирующий) ВВК, сопровождающееся> 4 рецидивов в течение 12 мес (табл. 1) [5]. Важно понимать, что рецидивирующий кандидоз отмечают в <5% женщин, его следует подтвердить посевом, а другие причины симптомов должны быть исключены путем дифференциальной диагностики. Важно также исключить сахарный диабет, ВИЧ-инфекцию или другие причины снижения иммунитета.
Таблица 1. Клиническая картина ВВК
| Клиническая презентация ВВК | |
|---|---|
| мужчины | женщины |
|
|
Микроскопический метод характеризуется забором мазка из влагалища для микроскопии окрашенного по Граму препарата и / или фазово-контрастной микроскопии влажного препарата. Интерпретация микроскопического анализа:
- наличие бластоспор, псевдогифы и нейтрофилов: инфекция, вызванная штаммами Candida;
- наличие только бластоспор и нейтрофилов: указывает на инфекцию, вызванную C. glabrata;
- наличие нейтрофилов в мазках из влагалища: признак воспалительного процесса (причиной которой может быть не только Candida)
- отсутствие нейтрофилов при наличии Candida: Указывает на носительство.
Скрининга на ВВК подлежат пациентки с жалобами на наличие выделений из влагалища, зуд, жжение, диспареунию, а также беременные. Скрининг проводят с помощью микроскопического исследования выделений влагалища. У беременных вульвовагинальное поражения грибами рода Candida повышает частоту развития осложнений беременности, в том числе преждевременных родов и внутриутробной гибели плода, а также повышением риска анте и интранатального инфицирования плода. Несмотря на выраженную клиническую картину ВВК, симптомы заболевания не является патогномоничным и требуют дифференциальной диагностики. Дифференциальную диагностику ВВК целесообразно проводить с такими заболеваниями, как бактериальный вагиноз, генитальный герпес, аэробный вагинит, кожными заболеваниями (экземой, красным плоским лишаем, склеродермией, болезнью Бехчета и др.). С этой целью, а также принимая во внимание возможность кандидоносительства, диагноз ВВК основывается на наличии типичных клинических проявлений с лабораторным подтверждением Candida в мазке из влагалища. В случае выявления Candida в ходе лабораторных исследований у женщины с симптомами ВВК необходимо применение соответствующей терапии, при отсутствии которой возможно вовлечение в патологический процесс мочеполовой системы (уретрит, цистит).
В соответствии с рекомендациями Британской ассоциации сексуального здоровья и ВИЧ (British Association for Sexual Health and HIV — BASHH) 2019 лечения ВВК зависит от формы заболевания и чувствительности к противогрибковым препаратам. Так, при остром ВВК рекомендовано назначение флуконазола или клотримазола, тогда как при резистентности Candida к флуконазолу рекомендуется назначение нистатина (рис. 2). Кроме того, при менеджменте пациентов с ВВК клиницист должен понимать, что эффективность лечения напрямую зависит от благосклонности самого пациента и соблюдением им всех рекомендованных врачом стратегий терапии (табл. 2) [6, 7].
Рисунок 2. Схема диагностики и лечения ВВГ
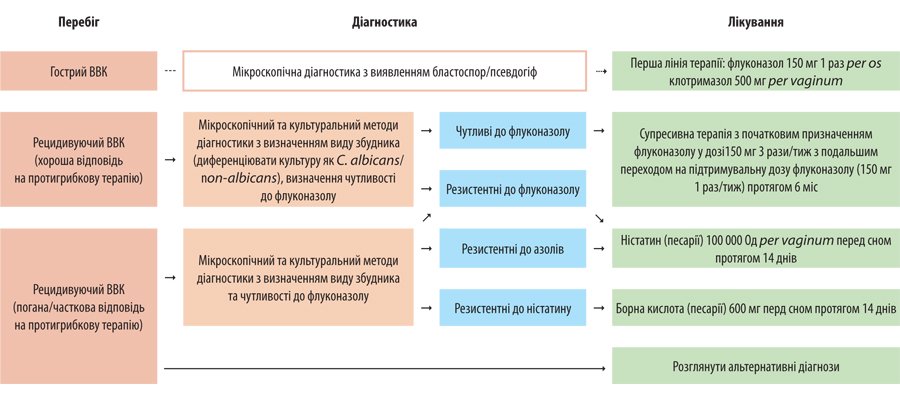
Таблица 2. Лечение ВВК в зависимости от формы заболевания
| Основные варианты лечения ВВК | |||
|---|---|---|---|
| форма ВВК | рекомендация | альтернатива | |
| острый | небеременных | Флуконазол 150 мг 1 раз / сутки per os, 1 раз per vaginum. Если пероральная терапия противопоказана, рекомендуется клотримазол 500 мг 1 per os, 1 раз per vaginum |
Клотримазол вагинальный крем (10%) 5 г 1 раз Клотримазол 1 вагинальная таблетка (пессарий) 200 мг 1 раз per vaginum перед сном 3 дня Эконазол 1 вагинальная таблетка (пессарий) 150 мг per vaginum 1 раз или 150 мг 1 раз per vaginum перед сном 3 дня Фентиконазол 1 капсула 600 мг per vaginum 1 раз или 200 мг 1 раз per vaginum перед сном 3 дня Итраконазол 200 мг per os 2 раза в сутки (1 день) Миконазол 1 вагинальная таблетка (пессарий) 1200 мг per vaginum 1 раз или 400 мг per vaginum перед сном 3 дня Миконазол вагинальный крем (2%) 5 г per vaginum перед сном 7 дней |
| беременные |
Клотримазол 1 вагинальная таблетка (пессарий) 500 мг per vaginum перед сном в течение 7 дней |
Клотримазол вагинальный крем (10%) 5 г перед сном до 7 дней Клотримазол 1 вагинальная таблетка (пессарий) 200 мг или 100 мг per vaginum перед сном 7 дней Эконазол 1 вагинальная таблетка (пессарий) 150 мг per vaginum перед сном 7 дней Миконазол 1 вагинальная таблетка (пессарий) 1200 мг или 400 мг per vaginum перед сном 7 дней Миконазол вагинальный крем (2%) 5 г per vaginum перед сном 7 дней |
|
| C. non-albicans и резистентные к азолов виды Candida | Нистатиновые вагинальные таблетки (пессарии) 100000 Ед. per vaginum перед сном в течение 14 дней |
Борная кислота суппозитории вагинальные 600 мг перед сном в течение 14 дней Амфотерицин В суппозитории вагинальные 50 мг перед сном в течение 14 дней Флуцитозина крем 5 г или 1 вагинальная таблетка (пессарий) 1 г с амфотерицином или нистатином per vaginum перед сном в течение 14 дней |
|
| Редицивуючий | небеременных |
Начальная терапия: флуконазол 150 мг per os каждые 72 ч (3 дозы) Поддерживающая терапия: флуконазол 150 мг per os 1 раз в неделю в течение 6 мес |
Начальная терапия: местная терапия имидазолом может быть продлена до 10-14 дней в зависимости от клинического ответа Поддерживающая терапия в течение 6 мес: клотримазол 1 вагинальная таблетка (пессарий) 500 мг per vaginum 1 раз в нед или итраконазол 50-100 мг per os ежедневно |
| беременные |
Индукция: местная терапия имидазолом может быть продлена до 10-14 дней в зависимости от клинического ответа Поддерживающая терапия: клотримазол (пессарий) 500 мг per vaginum еженедельно |
||
| C. non-albicans и резистентные к азолов виды Candida | Нистатиновые вагинальные таблетки (пессарии) 100000 Ед. per vaginum перед сном в течение 14 дней | Можно рассматривать альтернативные схемы в режиме 14 дней в месяц в течение 6 мес | |
Список использованной литературы:
- 1. Sobel JD (2007) Vulvovaginal candidosis. Lancet .; 369 (9577): 1961-71. doi: 10.1016 / S0140-6736 (07) 60917-9.
- 2. Mendling W., Brasch J., Cornely OA et al. (2015) uideline: vulvovaginal candidosis (AWMF 015/072), S2k (excluding chronic mucocutaneous candidosis). Mycoses .; 58 (Suppl. 1): 1-15. doi: 10.1111 / myc.12292.
- 3. Rodríguez-Cerdeira C., Gregorio MC, Molares-Vila A. et al. (2019) Biofilms and vulvovaginal candidiasis. Colloids Surf. B. Biointerfaces .; 174: 110-125. doi: 10.1016 / j.colsurfb.2018.11.011.
- 4. Cassone A. (2015) Vulvovaginal Candida albicans infections: pathogenesis, immunity and vaccine prospects. BJOG; 122 (6): 785-94. doi: 10.1111 / 1471-0528.12994.4.
- 5. The Australasian Sexual Health Alliance (2018) Candidiasis. Australian STI Management Guidelines, March 29.
- 6. Saxon Lead Author GDGC, Edwards A., Rautemaa-Richardson R, Owen C. et al. (2020) British Association for Sexual Health and HIV national guideline for the management of vulvovaginal candidiasis. Int J STD AIDS .; 31 (12): 1124-1144. doi: 10.1177 / 0956462420943034.
- 7. CDC (2015) Vulvovaginal Candidiasis. 2015 Sexually Transmitted Diseases Treatment Guidelines, June 4.
.
[ad_2]