Брутон также был первым врачом, который осуществил специфическую иммунотерапию этого Х-сцепленного расстройства путем введения инъекций IgG. Состояние пациента улучшилось, однако после сорока лет у него возникло хроническое обструктивное заболевание легких.
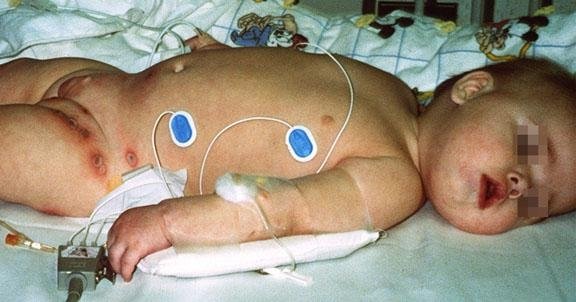
патофизиология
Сейчас это расстройство также называют Х-сцепленной агаммаглобулинемией (X-linked agammaglobulinemia — XLA), А генный дефект обнаружен в гене, который кодирует тирозинкиназы Брутона (BTK) на полосе Xq21.3. Ген BTK большой и состоит из 19 экзонов, кодирующих 659 аминокислот, которые образуют BTK цитозольного тирозинкиназы. Мутации могут происходить в любом участке гена. BTK необходим для пролиферации и дифференциации В-лимфоцитов.
При отсутствии функциональной BTK, зрелые В-клетки, которые экспрессируют поверхностный Ig и маркер CD19, отсутствуют. Отсутствие CD19 легко обнаружить с помощью флюороцитометричних анализов, и эта находка обычно легко подтверждает диагноз XLA у лиц мужского пола. Как сначала описал Брутон, XLA проявляется в 80% случаев как пневмония и другие бактериальные синопульмональни инфекции. Такие инфекции, начинающиеся у младенцев мужского пола, когда материнские антитела IgG, приобретенные трансплацентарно, теряются. Таким образом, XLA, скорее всего, диагностируется, когда у младенца мужского пола младше 1 года случаются необычно тяжелые или рецидивирующие синопульмональни инфекции.
У некоторых людей постановки диагноза затягивается до зрелого возраста. В некоторых случаях эту задержку можно объяснить разной степенью тяжести XLA, даже в семьях, в которых присутствует одинаковая мутация. Однако существенным фактором, способствующим, является плохая воспалительная реакция, которая наблюдается при отсутствии антител. Запоздалый диагноз ставит пациентов под угрозу хронической легочной болезни и плохого роста, что приводит к смертности в молодом возрасте.
При отсутствии зрелых В-клеток у пациентов не хватает лимфоидной ткани и не удается развиться плазматических клеток — то есть клеткам, которые производят антитела. Зародышевые центры, где В-клетки размножаются и дифференцируются, слабо развиты во всей лимфоидной ткани, включая селезенку. Миндалины, аденоиды, периферические лимфатические узлы и пятна Пейера в кишечнике — невелики или отсутствуют. В легких и кишечнике отсутствует нормальное распределение лимфоцитов. Однако биопсия исследования лимфоидной ткани и костного мозга в настоящее время не проводится в при обследовании в большинстве случаев XLA.
Эпидемиология
Ориентировочная рождаемость с XLA в США была рассчитана как 1 случай на 379 000 живорожденных. В Соединенных Штатах оценивается распространенность 1 случае на 250 000 человек. Однако это количество было рассмотрено до того, как стало доступным мутационное тестирование, и, как правило, считается заниженной. Считается, что новые мутации вызывают 30-50% случаев XLA.
![Bruton agammaglobulinemia (ie, X-linked agammaglobulinemia [XLA]) In brothers](https://hcv.com.ua/wp-content/uploads/2020/09/1600769670_306_Болезнь-Брутона-или-Х-сцепленный-агаммаглобулинемия.jpg)
смертность
Пациенты, получавшие внутривенно IgG (IVIG) до возраста 5 лет, имеют более низкие показатели заболеваемости и смертности, чем ранее выявленные пациенты, которые получали лечение только свежезамороженной плазмой (FFP) и внутримышечно Ig (IMIG) достичь уровня IgG около нормы или даже выше 200 мг / дл сложно с помощью FFP или IMIG. Пациенты, регулярно получающих терапию IVIG или подкожный IgG (SCIG), могут иметь почти нормальный образ жизни. Известно, что пациенты могут жить до семидесяти лет.
Вирусные и легочные инфекции вызывают более 90% смертности.
Хронические энтеровирусные инфекции является наиболее распространенной этиологии ранней заболеваемости. Высокие дозы IVIG, замедляют, но не прекращают, прогрессирование ухудшения функции ЦНС. Деменция, атаксия и парестезии являются общими клиническими признаками менингоэнцефалита, вызванного энтеровирусами. Другие вирусные причины смерти являются спорадическими. Аденовирусы являются общепризнанными причинами заболеваемости и смертности у любого пациента с ослабленным иммунитетом.
К общим возбудителей принадлежит S pneumoniae, H influenzae type b, and Staphylococcus aureus. Burkholderia cepacia и coagulase-negative staphylococci также важными возбудителями.
При наличии воспалительного заболевания кишечника, как правило, хронический характер XLA и приводит к гипотрофии и кахексии, а также увеличивает риск инфекции. Другие аутоиммунные расстройства, такие как артрит, могут быть особенно инвалидизирующими. Для пациентов с этими осложнениями обследование на наличие бактериальных возбудителей является важным, поскольку лечение иммунодепрессивными препаратами может осложнить лечение.
Пол
XLA — это расстройство, которое поражает только мужчин. Ни одной женщины-носителя с любым клиническим заболеванием, связанным с мутированным геном, не обнаружено.
Поскольку XLA является генетическим расстройством, младенцы мужского пола могут быть обследованы с помощью пренатальной диагностики, когда мать является носителем. Отбор проб ворсин хориона (CVS) можно проводить в начале беременности, а также анализ ДНК можно использовать, когда известна точная мутация в семье. Амниоцентез можно проводить позже в период гестации. Сбор фетальных лимфоцитов с помощью внутриутробного отбора проб из пуповины может быть использован для перечисления CD19 + В-клеток и зрелых Т-клеток с помощью флуороцитометричного анализа, хотя эта процедура ставит плод под определенный риск смертности (от <1-5%). При рождении пуповинную кровь можно направить на флюороцитометричний анализ популяций лимфоцитов. Количественный уровень IgG не важно, поскольку уровень IgG у плода в значительной степени отражает материнский IgG, транспортируется через плаценту.
От пассивного трансплацентарное переноса материнских IgG у новорожденных нормальный уровень IgG в сыворотке крови, и они могут не иметь проблем, пока IgG НЕ катаболизируется. Поскольку новорожденные не могут производить собственный Ig, повышенная восприимчивость к инфекциям обычно развивается у младенцев старше 6 месяцев. Итак, пациенты с XLA могут клинически проявляться в возрасте от 3 месяцев до 5 лет. Сейчас большинство случаев XLA оказываются у пациентов младше 1 года, в зависимости от скорости потери IgG от матери и возникновения инфекций. Средний возраст диагноза младший у пациентов с семейным анамнезом (2,6 года), чем у пациентов без него (5,4 года).
Пациенты могут также наблюдаться во втором или третьем десятилетии жизни, хотя это случается редко. Старший возраст на момент установления диагноза — 51 год. У этих пациентов может быть легче проявление заболевания, связанный с наличием мутировавшего белка BTK, а не полное отсутствие белка. В редких случаях человек страдает легкой формой заболевания, тогда как другие с такой же мутацией имеют более серьезные клинические заболевания.
